En 2013, 81 centres français ont réalisé des greffes de cellules souches hématopoïétiques (CSH). Cette activité est divisée en deux catégories : greffes allogéniques et greffes autologues. L’activité de greffe allogénique est la seule soumise à autorisation. Parmi ces 81 centres, 44 n’ont réalisé que des autogreffes, 4 n’ont réalisé que des allogreffes et 33 ont eu une activité mixte.
En 2013, 4 757 patients ont reçu une ou plusieurs injections de CSH autologues ou allogéniques, soit 2 911 patients autogreffés et 1 846 patients allogreffés. L’analyse de l’activité 2013 (tableau CSH G1), montre une augmentation de 10% du nombre des greffes autologues par rapport à 2012, qui ramène ce nombre au même niveau qu’en 2010, et une augmentation de 8,8% du nombre de greffes allogéniques.
Tableau CSH G1. Evolution du nombre de greffes de CSH
|
2004 |
2005 |
2006 |
2007 |
2008 |
2009 |
2010 |
2011 |
2012 |
2013 |
Nombre de greffes autologues |
3176 |
3121 |
2949 |
2860 |
2951 |
2675 |
3047 |
3003 |
2766 |
3044 |
Nombre de greffes allogéniques |
982 |
1205 |
1252 |
1379 |
1472 |
1539 |
1656 |
1772 |
1721 |
1872 |
dont greffes non apparentées |
311 |
513 |
623 |
765 |
841 |
902 |
937 |
1023 |
1011 |
1090 |
Nombre total de greffes |
4158 |
4326 |
4201 |
4239 |
4423 |
4214 |
4703 |
4775 |
4487 |
4916 |
Source : déclarations d’activité des centres de greffe
Matériel et méthodes
Données
Mode de recueil
Depuis 1995, l’Etablissement français des Greffes, puis l’Agence de la biomédecine, recueille chaque année deux types d’informations relatives aux greffes : le nombre total de greffes réalisées et le nombre total de patients greffés, par centre et par type de greffe (ces chiffres sont reportés dans les Tableaux CSH G2, CSH G9, CSH G10) et des informations plus précises concernant chaque nouvelle greffe réalisée pendant l’année en cours, ainsi que la mise à jour du suivi des patients greffés les années précédentes.
Le nombre total de greffes réalisées et le nombre total de patients greffés sont obtenus d’une part par les fiches papier d’activité recueillies auprès de chaque centre, et d’autre part par extraction de la base ProMISe (base de données de l’EBMT, gérée à Londres). Lors du contrôle qualité effectué par l’Agence de la biomédecine, ces deux sources de données sont comparées et en cas de discordance, des demandes de correction sont envoyées aux centres de greffe. Par ailleurs le nombre de greffes allogéniques non apparentées (tableaux CSH G8, CSH G10, figure CSH G6) est comparé pour chaque centre au nombre de prélèvements de greffons de CSH réalisés pour des patients français et recensés par le Registre France Greffe de Moelle (tableaux RFGM 1, RFGM 4, RFGM 7). Les discordances qui persistent après contrôle auprès des centres sont dues essentiellement au fait que certains greffons ne sont finalement pas infusés en raison de l’état du patient, ou que certains greffons constitués en fin d’année sont infusés au début de l’année suivante (cas des greffons de sang placentaire) ou encore au fait que des fractions de greffons prélevés les années antérieures ont été congelées puis infusées plus tardivement aux patients.
Population étudiée - Exhaustivité
La base de données constituée par l’extraction des données saisies dans ProMISe par les 81 centres de greffe de CSH comprend pour les greffes 2013 :
11 686 allogreffes réalisées pour 1 662 patients ; l’exhaustivité est de 90,1% par rapport aux chiffres d’activité communiqués par les centres (Tableaux CSH G9 et CSH G10) ;
2 176 autogreffes réalisées sur 2 071 patients ; l’exhaustivité est de 71,5% (Tableau CSH G2).
Pour l’étude de la survie des patients après allogreffe de CSH, la base de données contient 20 356 patients ayant reçu une allogreffe entre 1995 et 2013. Parmi eux, ont été exclus ceux dont l’une des variables de suivi (état aux dernières nouvelles ou date de dernières nouvelles) était manquante, soit 123 patients (0,6%). La base finale contenait donc 20 233 patients, dont 11 191 (55,3%) allogreffés à partir d’un donneur apparenté, 8 963 (44,3%) allogreffés à partir d’un donneur non apparenté et 79 (0,4%) pour lesquels le type de donneur était manquant. Selon la sous-population étudiée, cette base de données a été conservée dans son entier ou bien réduite à une cohorte plus récente (2001-2013).
Le suivi des patients dans ProMISe est saisi grâce à l’état aux dernières nouvelles et à la date de dernières nouvelles, qui sont écrasés au fur et à mesure de leur mise à jour. Le critère étudié est le délai entre la date de greffe et la date de dernières nouvelles. En cas de décès, la date de dernières nouvelles est la date du décès. La plupart des centres de greffe suit les patients allogreffés annuellement pendant au moins 5 ans après la greffe. Au-delà de 5 ans, les patients sont parfois suivis uniquement en ville et leur suivi après 5 ans ne peut donc être saisi dans ProMISe. Pour connaître la qualité du suivi des patients dans ProMISe, nous avons choisi de calculer trois indicateurs : le pourcentage de suivis manquants à 1 an, 3 ans et 5 ans. Le pourcentage de suivis manquants à 1 an se calcule sur la cohorte des patients allogreffés entre 1995 et 2012 (pour lesquels on dispose d’un recul d’au moins 1 an après la greffe). Parmi ces patients, certains ont une date de dernière nouvelles au-delà de 1 an post-greffe (que cela corresponde à l’état décédé ou vivant), d’autres sont indiqués morts avant 1 an, et d’autres sont indiqués vivants avant 1 an. Ce sont ces derniers qui sont considérés comme ayant un suivi manquant à 1 an. On procède de même pour calculer le pourcentage de suivis manquants à 3 ans (sur la cohorte des patients pour lesquels on a au moins trois ans de recul : patients allogreffés entre 1995 et 2010) et le pourcentage de suivis manquants à 5 ans (sur la cohorte des patients allogreffés entre 1995 et 2008). Dans la base extraite de ProMISe en mai 2014, le pourcentage de suivis manquants à 1 an est de 6%. Les suivis manquants à 1 an concernent, à 69%, des greffes réalisées de 2011 à 2012. Le pourcentage de suivis manquants à 3 ans est de 10%. Les suivis manquants à 3 ans concernent, à 71%, des greffes réalisées de 2006 à 2010. Le pourcentage de suivis manquants à 5 ans est de 14%. Les suivis manquants à 5 ans concernent, à 72%, des greffes réalisées de 2004 à 2008. Cela montre bien le retard de saisie des suivis dans la base ProMISe.
Méthodes statistiques
Les résultats présentés sur les greffes de l’année 2013 ont été obtenus à l’aide des procédures de statistique descriptive du logiciel SAS (version 9.2).
Pour l’étude de la survie des patients après allogreffe de CSH, le critère étudié est la durée de survie du patient après la greffe quel que soit le nombre de greffes reçues. Pour un patient ayant reçu plusieurs greffes, il est défini comme le délai entre la date de la première greffe, et la date des dernières nouvelles de la dernière greffe. On regarde également l’état du patient à la date de dernières nouvelles (vivant / décédé). La date de point a été fixée au 23 mai 2014. Si la date de dernières nouvelles dépasse la date de point, le patient sera considéré vivant à la date de point. Les courbes de survie ont été réalisées par la méthode actuarielle et les estimations de la probabilité de survie à différents délais ont été calculées par la méthode de Kaplan-Meier. Pour chaque courbe est également indiquée la médiane de survie, c’est-à-dire le temps au bout duquel 50% des patients sont encore en vie.
Ces résultats sont à interpréter avec prudence. Ils ne donnent qu’une idée globale de la survie des patients après allogreffe de CSH. En effet, la plupart des courbes représentées ne prennent en compte qu’un seul facteur : l’indication de la greffe. Pour apprécier plus précisément l’efficacité de la greffe, il est indispensable de tenir compte de l’ensemble des facteurs pronostiques potentiels.
Activité d’autogreffe globale
En 2013, 3 044 greffes autologues ont été réalisées pour 2 911 patients qui ont reçu une ou plusieurs autogreffes. En 2009, dix centres d’autogreffe n’avaient pas déclaré leur activité. Le nombre de patients autogreffés était donc probablement sous-estimé. En revanche, en 2013, tous les centres ont déclaré leur activité d’autogreffe. Les chiffres sur les 10 dernières années montrent que malgré quelques fluctuations en plus (en 2004, 2008, 2010-2011 et 2013) ou en moins (2009, 2012), l’activité d’autogreffe est globalement stable autour de 2600 à 2900 patients autogreffés par an (Figure CSH G1).
Les greffes autologues ont été réalisées par 77 équipes, parmi lesquelles 25 ont réalisé chacune 50 autogreffes ou plus et 13 équipes moins de 10 autogreffes. Dans 99,6% des cas le greffon est constitué de cellules souches hématopoïétiques issues du sang périphérique.
Le tableau CSH G2 rapporte l’activité d’autogreffe telle qu’elle a été déclarée par chaque centre. Dans la colonne centrale est notée l’activité extraite de la base de données ProMISe. En grisé sont indiqués les centres qui ont saisi dans ProMISe moins des trois quarts des greffes réalisées. Par ailleurs, malgré le contrôle qualité effectué sur la base ProMISe, il persiste deux centres pour lesquels le nombre de greffes saisies est légèrement supérieur au nombre de greffes déclarées.
L’âge moyen des patients recevant une greffe de CSH autologue est de 52 ans. L’âge médian de ces patients est de 57 ans et 14,5% d’entre eux ont plus de 65 ans (Figure CSH G2).
Indications thérapeutiques
En 2013, le nombre de patients ayant reçu une autogreffe dont les données sont saisies dans la base de données européenne ProMISe est de 2 071. Mille huit cent quatre-vingt patients (1 880) ont été traités dans le cadre d’hémopathies essentiellement malignes (91,2%), 185 (soit 8,6%) dans le cadre d’une tumeur solide et 6 patients (0,2%) ont été traités dans le cadre d’une maladie autoimmune (Tableau CSH G4, Tableau CSH G5, Figure CSH G3, Figure CSH G4).
Les lymphomes non hodgkiniens (LNH) et les myélomes représentent respectivement 34,8% et 47,1% des indications d’autogreffe, et sont donc les indications majeures d’autogreffe (Figure CSH G5-a). Les indications d’autogreffe pour LAM restent très faibles numériquement (Figure CSH G5-b). La part du cancer du sein est stable et représente 1,2% des indications totales d’autogreffe (Figure CSH G5-c) et 13% des indications non hématologiques (Figure CSH G4). Les autres indications sont stables.
Figure CSH G1. Evolution du nombre de patients ayant eu une autogreffe de CSH
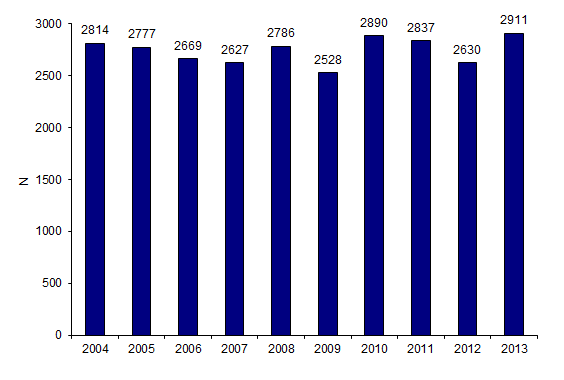
Source : déclarations d’activité des centres de greffe
Tableau CSH G2. Evolution de l'activité d'autogreffe de CSH par équipe
|
Nombre d'autogreffes |
ProMISe |
Nombre de patients |
||||||
|
2010 |
2011 |
2012 |
2013 |
2013 |
2010 |
2011 |
2012 |
2013 |
Amiens Hôpital Sud |
41 |
37 |
52 |
44 |
44 |
41 |
37 |
52 |
44 |
Angers Centre Paul Papin |
8 |
8 |
0 |
10 |
0 |
3 |
4 |
0 |
4 |
Angers CHU |
35 |
46 |
34 |
61 |
61 |
35 |
41 |
33 |
50 |
Argenteuil CH Victor Dupouy |
18 |
22 |
19 |
28 |
1 |
18 |
22 |
18 |
28 |
Bayonne Centre Hospitalier |
14 |
8 |
23 |
23 |
23 |
14 |
8 |
23 |
23 |
Besançon Hôpital Jean Minjoz |
57 |
48 |
47 |
52 |
51 |
55 |
43 |
42 |
49 |
Bobigny Hôpital Avicenne |
26 |
18 |
29 |
27 |
0 |
25 |
18 |
29 |
27 |
Bordeaux Groupe Hospitalier Pellegrin |
10 |
14 |
5 |
6 |
6 |
8 |
12 |
4 |
4 |
Bordeaux Pessac Hôpital Haut Lévêque |
113 |
83 |
111 |
119 |
119 |
111 |
79 |
108 |
119 |
Boulogne/Mer Hôpital Duchenne |
12 |
14 |
7 |
12 |
12 |
12 |
13 |
7 |
12 |
Brest Hôpital Augustin Morvan |
30 |
40 |
19 |
37 |
30 |
29 |
38 |
19 |
32 |
Caen Centre Régional François Baclesse |
30 |
45 |
25 |
12 |
0 |
29 |
41 |
24 |
12 |
Caen CHU |
30 |
35 |
39 |
47 |
43 |
30 |
35 |
38 |
47 |
Clamart Hôpital d'Instruction des Armées |
16 |
33 |
31 |
42 |
3 |
13 |
31 |
30 |
42 |
Clermont-Ferrand |
84 |
65 |
74 |
66 |
4 |
75 |
64 |
71 |
63 |
Colmar Hôpital Louis Pasteur |
5 |
9 |
8 |
10 |
0 |
5 |
8 |
8 |
10 |
Corbeil Hôpital Gilles de Corbiel |
21 |
19 |
10 |
13 |
1 |
21 |
18 |
10 |
12 |
Créteil Hôpital Henri Mondor |
0 |
1 |
1 |
1 |
1 |
0 |
1 |
1 |
1 |
- unité Hémopathies Lymphoïdes |
28 |
27 |
25 |
28 |
28 |
28 |
27 |
25 |
28 |
Dijon Hôpital Le Bocage |
108 |
86 |
91 |
109 |
110* |
95 |
74 |
76 |
109 |
Dunkerque Centre Hospitalier |
13 |
10 |
15 |
15 |
15 |
13 |
10 |
15 |
15 |
Grenoble CHU |
52 |
42 |
33 |
44 |
44 |
49 |
42 |
33 |
43 |
Lens Centre Hospitalier |
13 |
21 |
12 |
13 |
0 |
13 |
21 |
12 |
13 |
Lille Centre Hospitalier Saint-Vincent |
15 |
22 |
19 |
10 |
10 |
15 |
22 |
19 |
10 |
Lille Centre Oscar Lambret |
13 |
27 |
9 |
18 |
0 |
12 |
17 |
8 |
13 |
Lille CHU Claude Huriez |
49 |
36 |
30 |
40 |
39 |
49 |
36 |
30 |
40 |
Lille Hôpital Jeanne de Flandre |
3 |
0 |
3 |
0 |
0 |
2 |
0 |
3 |
0 |
Limoges Centre Hospitalier Dupuytren |
34 |
30 |
39 |
33 |
21 |
34 |
30 |
39 |
33 |
Lyon Centre Hospitalier Lyon Sud |
113 |
102 |
92 |
110 |
110 |
111 |
102 |
92 |
110 |
- service d'hématologie secteur 1G |
8 |
3 |
2 |
0 |
0 |
7 |
3 |
2 |
0 |
Lyon CRLC Léon Bérard |
81 |
94 |
68 |
78 |
78 |
73 |
80 |
57 |
68 |
Lyon Institut d'Hématologie et d'Oncologie Pédiatrique |
17 |
16 |
12 |
16 |
16 |
16 |
14 |
8 |
14 |
Marseille Hôpital de la Conception |
/ |
/ |
/ |
14 |
0 |
/ |
/ |
/ |
14 |
Marseille Hôpital de la Timone |
7 |
14 |
1 |
5 |
5 |
5 |
13 |
1 |
5 |
Marseille Institut Paoli Calmettes |
217 |
205 |
175 |
178 |
178 |
204 |
188 |
164 |
168 |
Meaux Centre Hospitalier |
11 |
12 |
19 |
17 |
7 |
11 |
12 |
18 |
16 |
Metz Hôpital Notre Dame de Bon Secours |
22 |
31 |
27 |
28 |
0 |
22 |
30 |
27 |
28 |
Montpellier Hôpital Saint-Eloi et Hôpital Arnaud de Villeneuve |
88 |
80 |
87 |
76 |
75 |
84 |
77 |
87 |
75 |
Mulhouse Hôpital Emile Muller |
20 |
12 |
15 |
21 |
21 |
19 |
12 |
14 |
21 |
Nancy Hôpital d’Adultes |
56 |
76 |
51 |
56 |
56 |
54 |
75 |
51 |
56 |
Nancy Hôpital d'Enfants |
6 |
11 |
10 |
6 |
6 |
6 |
7 |
9 |
4 |
Nantes Hôtel Dieu |
127 |
128 |
126 |
124 |
124 |
127 |
127 |
126 |
124 |
Nice Centre Antoine Lacassagne |
46 |
47 |
51 |
60 |
21 |
46 |
46 |
51 |
60 |
Nice Hôpital de l'Archet 1 |
35 |
29 |
19 |
22 |
10 |
33 |
29 |
18 |
22 |
Orléans CHR |
/ |
/ |
/ |
12 |
12 |
/ |
/ |
/ |
12 |
Paris Hôpital Cochin |
55 |
52 |
62 |
68 |
0 |
54 |
52 |
62 |
65 |
Paris Hôpital d'Enfants Armand Trousseau |
11 |
5 |
5 |
3 |
3 |
10 |
5 |
5 |
3 |
Paris Hôpital Necker |
38 |
41 |
32 |
36 |
37* |
38 |
41 |
32 |
36 |
- unité d'Hémato-Immunologie Pédiatrique |
2 |
5 |
3 |
2 |
1 |
2 |
5 |
3 |
1 |
Paris Hôpital Robert Debré |
0 |
2 |
2 |
0 |
0 |
0 |
2 |
2 |
0 |
Paris Hôpital Saint-Antoine |
52 |
47 |
44 |
63 |
19 |
50 |
46 |
44 |
63 |
Paris Hôpital Saint-Louis |
0 |
3 |
2 |
3 |
3 |
0 |
3 |
2 |
3 |
- service d’Onco-Hématologie |
62 |
56 |
41 |
29 |
0 |
60 |
56 |
41 |
29 |
- service d'Hématologie Adulte |
5 |
4 |
1 |
1 |
0 |
5 |
4 |
1 |
1 |
- service d’Immuno-Hématologie 1 |
57 |
61 |
NC§ |
54 |
0 |
57 |
61 |
NC§ |
54 |
Paris Hôpital Tenon |
43 |
50 |
26 |
35 |
33 |
24 |
41 |
15 |
17 |
Paris Hôtel Dieu |
26 |
/ |
/ |
/ |
/ |
25 |
/ |
/ |
/ |
Paris Institut Curie |
46 |
47 |
40 |
50 |
1 |
46 |
47 |
40 |
46 |
Paris La Pitié Salpetrière |
55 |
54 |
59 |
54 |
54 |
54 |
54 |
59 |
53 |
Poitiers Hôpital Jean Bernard |
45 |
55 |
58 |
48 |
48 |
45 |
54 |
58 |
48 |
Pontoise CH René Dubos |
20 |
18 |
12 |
17 |
0 |
20 |
18 |
12 |
17 |
Reims Hôpital Robert Debré |
51 |
47 |
39 |
53 |
52 |
51 |
47 |
39 |
53 |
Rennes CHU |
89 |
102 |
84 |
119 |
9 |
87 |
97 |
81 |
113 |
Roubaix Hôpital Provo |
16 |
18 |
13 |
14 |
0 |
16 |
17 |
13 |
14 |
Rouen Centre Henri Becquerel |
54 |
73 |
60 |
64 |
63 |
52 |
70 |
58 |
63 |
Rouen Hôpital Charles Nicolle |
3 |
9 |
6 |
4 |
4 |
3 |
6 |
6 |
4 |
Saint-Cloud Centre René Huguenin |
47 |
25 |
33 |
39 |
39 |
46 |
25 |
32 |
39 |
Saint-Denis (Réunion) CHD Félix Guyon |
11 |
14 |
15 |
11 |
0 |
11 |
14 |
15 |
11 |
Saint-Étienne |
44 |
36 |
34 |
41 |
39 |
43 |
34 |
33 |
41 |
Saint-Pierre (Réunion) CH François Dunan |
0 |
11 |
10 |
8 |
0 |
0 |
11 |
10 |
7 |
Saint Quentin Centre Hospitalier |
10 |
14 |
14 |
8 |
2 |
10 |
14 |
14 |
8 |
Strasbourg Hôpital de Hautepierre |
60 |
64 |
96 |
73 |
73 |
58 |
63 |
81 |
71 |
Toulouse Hôpital Purpan |
9 |
18 |
5 |
11 |
9 |
5 |
13 |
5 |
8 |
- service d'Hématologie |
103 |
73 |
93 |
119 |
119 |
103 |
72 |
91 |
118 |
Toulouse Institut Claudius Regaud |
6 |
9 |
3 |
6 |
0 |
3 |
4 |
1 |
2 |
Tours Hôpital Bretonneau |
87 |
98 |
79 |
62 |
32 |
87 |
95 |
72 |
61 |
Valenciennes Hôtel Dieu |
15 |
13 |
8 |
14 |
0 |
15 |
13 |
8 |
14 |
Versailles Hôpital André Mignot |
20 |
28 |
44 |
29 |
0 |
20 |
28 |
44 |
29 |
Villejuif Hôpital Paul Brousse |
6 |
5 |
7 |
7 |
7 |
4 |
4 |
5 |
7 |
Villejuif Institut Gustave Roussy : |
99 |
85 |
101 |
97 |
85 |
87 |
77 |
97 |
90 |
- service d'Oncologie Pédiatrique |
68 |
55 |
70 |
59 |
59 |
47 |
37 |
47 |
42 |
Total |
3047 |
3003 |
2766 |
3044 |
2176 |
2890 |
2837 |
2630 |
2911 |
§ Activité non communiquée
* Nombre d'autogreffes saisies supérieur au nombre déclaré
Source : déclarations d’activité des centres de greffe
Tableau CSH G3. Evolution de l’activité d’autogreffe de CSH au niveau des schémas interrégionaux d’organisation sanitaire (SIOS)
|
Nombre d'autogreffes |
Nombre de patients |
||||||
|
2010 |
2011 |
2012 |
2013 |
2010 |
2011 |
2012 |
2013 |
SIOS Nord-Ouest |
317 |
374 |
312 |
315 |
312 |
352 |
307 |
309 |
SIOS Ouest |
421 |
477 |
400 |
473 |
413 |
456 |
389 |
444 |
SIOS Sud -Ouest |
289 |
235 |
279 |
317 |
278 |
218 |
271 |
307 |
SIOS Est |
385 |
384 |
384 |
408 |
365 |
359 |
347 |
401 |
SIOS Sud-Est |
399 |
358 |
315 |
355 |
374 |
339 |
296 |
339 |
SIOS Sud-Méditerranée |
393 |
375 |
333 |
355 |
372 |
353 |
321 |
344 |
SROS Ile de France |
832 |
775 |
718 |
802 |
765 |
735 |
674 |
749 |
SROS Réunion |
11 |
25 |
25 |
19 |
11 |
25 |
25 |
18 |
France |
3047 |
3003 |
2766 |
3044 |
2890 |
2837 |
2630 |
2911 |
Source : déclarations d’activité des centres de greffe
Figure CSH G2. Evolution de l'âge moyen des patients ayant eu une autogreffe de CSH
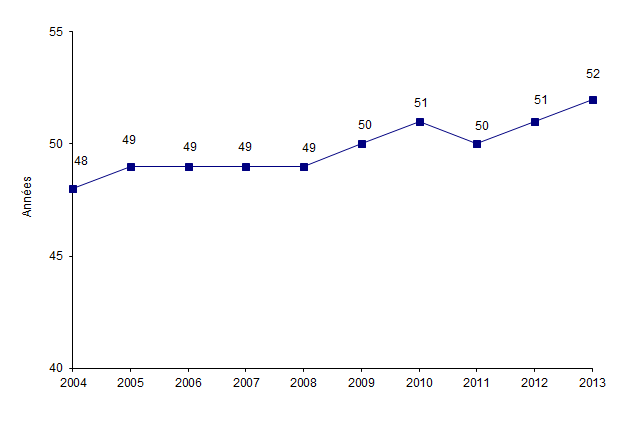
Source : Base ProMISe (extraction du 5 mai 2014)
Tableau CSHG4. Evolution de l’activité d’autogreffe de CSH, selon le type d’indication
|
2005 |
2006 |
2007 |
2008 |
2009 |
2010 |
2011 |
2012 |
2013 |
Nombre de greffes autologues |
3121 |
2949 |
2860 |
2951 |
2675 |
3047 |
3003 |
2766 |
3044 |
Nombre de patients |
2772 |
2669 |
2627 |
2786 |
2528 |
2890 |
2837 |
2630 |
2911 |
Proportion d'hémopathies (%) |
88,5 |
88,6 |
88,8 |
89,4 |
90,2 |
90,5 |
89,2 |
91,2 |
90,8 |
Proportion de tumeurs solides (%) |
11,5 |
11,4 |
10,9 |
10,3 |
9,5 |
9,3 |
10,6 |
8,6 |
8,9 |
Proportion de maladie auto-immune (%) |
0 |
0 |
0,3 |
0,3 |
0,3 |
0,2 |
0,2 |
0,2 |
0,3 |
Source : Base ProMISe (extraction du 5 mai 2014)
Tableau CSH G5. Répartition des autogreffes en 2013, selon le type de pathologie, par région administrative
|
Hémopathies essentiellement malignes (%) |
Tumeurs solides (%) |
Maladies Auto-immunes (%) |
Alsace |
90,2 |
9,8 |
0,0 |
Aquitaine |
96,6 |
3,5 |
0,0 |
Auvergne* |
0,0 |
100,0 |
0,0 |
Basse Normandie |
100,0 |
0,0 |
0,0 |
Bourgogne |
98,0 |
0,0 |
2,0 |
Bretagne |
81,1 |
18,9 |
0,0 |
Centre |
95,4 |
4,7 |
0,0 |
Champagne-Ardenne |
98,1 |
1,9 |
0,0 |
Franche-Comté |
95,8 |
4,2 |
0,0 |
Haute Normandie |
93,9 |
6,1 |
0,0 |
Ile-de-France |
81,7 |
17,7 |
0,6 |
Languedoc-Roussillon |
92,0 |
8,0 |
0,0 |
Limousin |
100,0 |
0,0 |
0,0 |
Lorraine |
95,0 |
5,0 |
0,0 |
Midi-Pyrénées |
94,4 |
4,8 |
0,8 |
Nord-Pas-de-Calais |
98,7 |
0,0 |
1,3 |
Pays de la Loire |
89,6 |
10,4 |
0,0 |
Picardie |
100,0 |
0,0 |
0,0 |
Poitou-Charentes |
95,8 |
4,2 |
0,0 |
Provence-Alpes-Côte d'Azur |
83,8 |
16,2 |
0,0 |
Rhône alpes |
91,6 |
8,4 |
0,0 |
France |
90,8 |
8,9 |
0,3 |
Source : Base ProMISe (extraction du 5 mai 2014)
*Chiffres à considérer avec prudence car seules 4 autogreffes parmi les 66 réalisées à Clermont-Ferrand ont été saisies dans Promise.
Par ailleurs, La Réunion n'apparaît pas dans ce tableau car aucune des 19 autogreffes réalisées à La Réunion n'a été saisie.
Figure CSH G3. Répartition des diagnostics chez les patients ayant eu une autogreffe de CSH en 2013 (hémopathies)
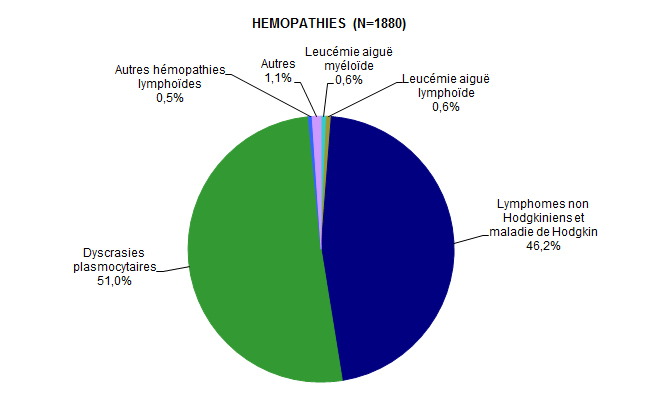
Source : Base ProMISe (extraction du 5 mai 2014)
Figure CSH G4. Répartition des diagnostics chez les patients ayant eu une autogreffe de CSH en 2013 (tumeurs solides)
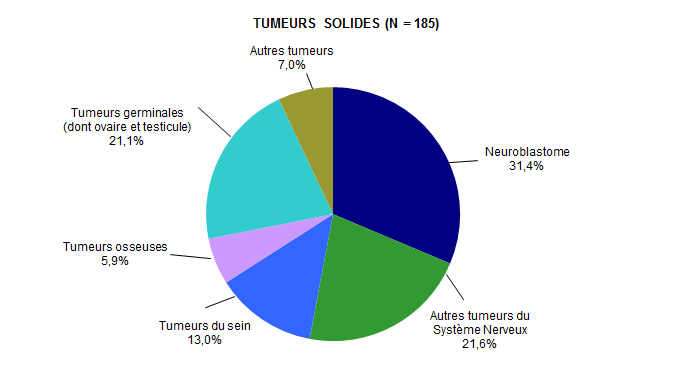
Source : Base ProMISe (extraction du 5 mai 2014)
Figure CSH G5a. Evolution de la répartition des indications d’autogreffe
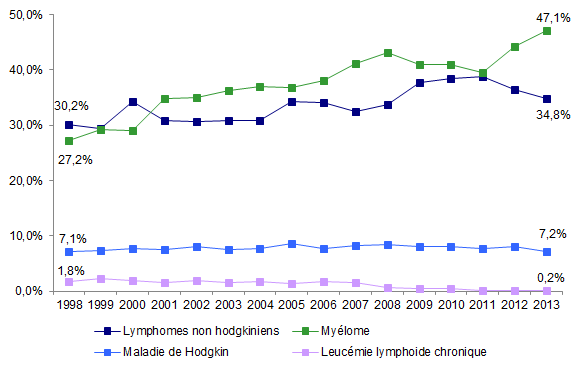
Source : Base ProMISe (extraction du 5 mai 2014)
Figure CSH G5b. Evolution de la répartition des indications d’autogreffe
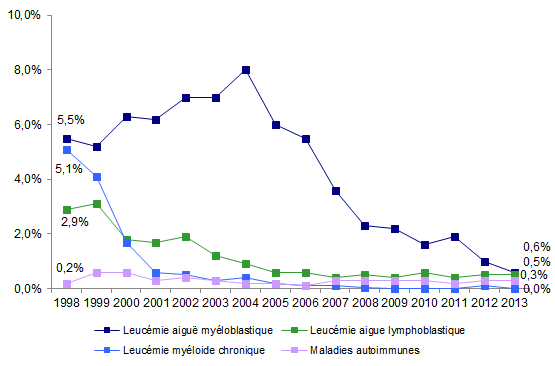
Source : Base ProMISe (extraction du 5 mai 2014)
Figure CSH G5c. Evolution de la répartition des indications d’autogreffe
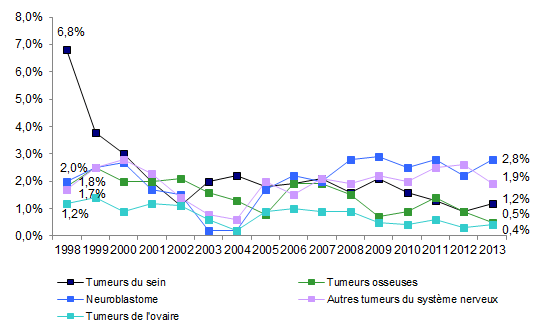
Source : Base ProMISe (extraction du 5 mai 2014)
Autogreffe pédiatrique
En 2013, les autogreffes pédiatriques ont été réalisées dans 22 centres (d’après les données saisies dans la base ProMISe). Elles diminuent en valeur relative (5,6% des autogreffes en 2013 contre 8,2% en 2012, 9% en 2011, 6,9% en 2010, 8,2% en 2009 et 8,2% en 2008) mais sont stables en valeur absolue (171 greffes en 2013 contre 176 en 2012, 215 en 2011, 175 en 2010, 203 en 2009 et 2008), tandis que la moyenne d’âge des enfants autogreffés est stable (7 ans en 2013 et 2012 contre 6,8 ans en 2011 et 6,9 ans en 2010). Le tableau CSH G6 et le tableau CSH G7 donnent la répartition des 129 enfants autogreffés en 2013 selon l’âge et le type d’indication.
Tableau CSH G6. Répartition des 129 enfants autogreffés en 2013 selon l’âge
Classe d'âge |
Nombre d'enfants |
0 - 5 ans |
73 |
6 - 10 ans |
26 |
11 - 15 ans |
17 |
16 - 18 ans |
13 |
Total |
129 |
Source : Base ProMISe (extraction du 5 mai 2014)
Tableau CSH G7. Répartition des 129 enfants autogreffés en 2013 selon le type d’indication
Type d'indication |
Nombre d'enfants |
Hémopathies malignes |
14 |
Tumeurs solides |
114 |
Déficit immunitaire |
1 |
Total |
129 |
Source : Base ProMISe (extraction du 5 mai 2014)
Activité globale de greffe allogénique
En 2013, 1 872 greffes de CSH allogéniques (moelle osseuse, sang périphérique ou sang placentaire) ont été réalisées chez 1 846 patients. Il s’agissait de 782 greffes avec un donneur apparenté et de 1 090 greffes avec un donneur non apparenté (Tableau CSH G8).
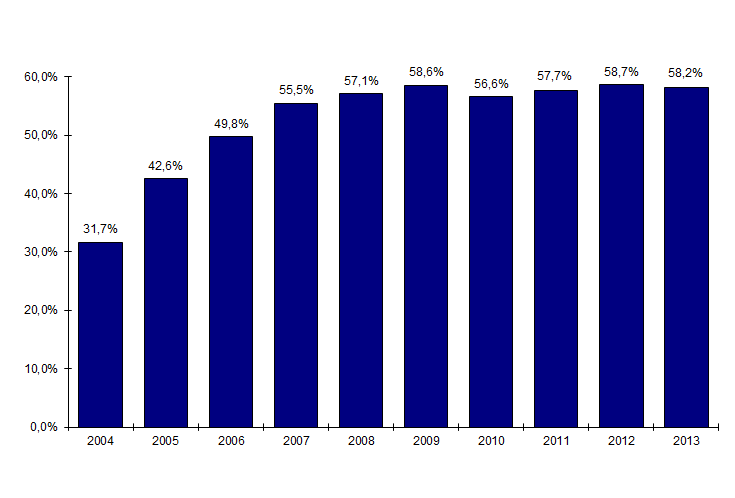
L’activité d’allogreffe de CSH est depuis plusieurs années en progression constante en nombre absolu, et ce principalement en raison de l’augmentation des allogreffes non apparentées : les greffes non apparentées sont majoritaires depuis 2007, et représentent plus de 58% des allogreffes en 2013 (Figure CSH G7).
Il est à noter qu’à l’intérieur de l’activité de greffes non apparentées, celles réalisées avec donneur adulte volontaire provenant du fichier national ou international est en progression continue depuis dix ans : de 242 greffes en 2004 à 902 en 2013, soit une progression de presque 300%. En 2013 comme en 2012, c’est donc l’activité de greffe non apparentée de sang placentaire qui a diminué par comparaison à 2011 (cf paragraphes suivants), tandis que celle de donneurs adultes continuait de progresser, essentiellement du fait de l’augmentation du nombre des donneurs sur les fichiers internationaux, ce qui augmente la probabilité pour chaque patient d’identifier un donneur compatible dit « phéno-identique » ou « 10/10 ».
Le nombre de greffes non apparentées évalué dans la base ProMISe est de 982, contre 1 090 greffes déclarées dans les fiches d’activité (Figure CSH G8). Le nombre de greffes apparentées évalué dans la base ProMISe est de 703, contre 782 greffes déclarées dans les fiches d’activité. Sous l’hypothèse que les chiffres déclarés sont exacts, on en déduit que 9,9% des greffes non apparentées et 10,1% des greffes apparentées n’ont pas été saisies ou ont été saisies avec parenté manquante.
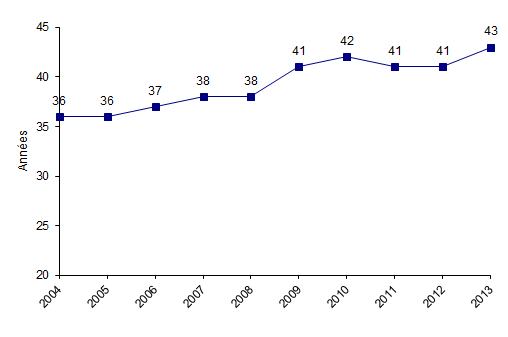
L’âge moyen des patients allogreffés est en augmentation (Figure CSH G9). Il est de 43 ans en 2013 contre 41 ans en 2012 et 2011 et si l’on exclut les patients de moins de 18 ans, l’âge moyen en 2013 est de 49 ans contre 48 en 2009, 2010 et 2011.
Il est important de noter que 36,4% des patients greffés ont plus de 55 ans, contre 33% en 2012 et 2011 et 26,9% en 2008) ; ceci est à rapprocher du nombre de greffes réalisées après un conditionnement non myéloablatif (Figure CSH G16), qui s’adressent à des patients plus âgés et/ou présentant des comorbidités : 59,1% de greffes réalisées avec un conditionnement non myéloablatif en 2013 contre 53,6% en 2012.
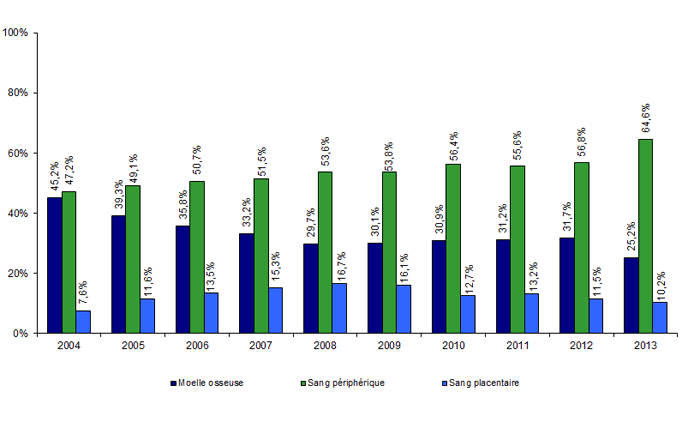
Depuis 2004, la source principale de greffons allogéniques est le sang périphérique et la part représentée par ces greffons progresse en 2013 (64,6% contre 56,8% en 2012). Cette prépondérance (Figure CSH G10) reste liée à celle de la greffe avec conditionnement d’intensité réduite et à celle de la greffe non apparentée, dans la mesure où un certain nombre de registres étrangers privilégient ce mode de recueil des CSH. Parallèlement, la part des greffons médullaires baisse légèrement (471 en 2013 pour 546 en 2012, 552 en 2011, 521 en 2010, 463 en 2009 et 437 en 2008) mais reste non négligeable en raison de leur utilisation élective dans un certain nombre d’indications, comme les aplasies médullaires ou dans de nombreuses indications pédiatriques, et du risque de réaction du greffon contre l’hôte chronique supérieur avec les CSH périphériques, maintenant bien identifié grâce aux méta-analyses des essais cliniques randomisés entre greffe de moelle et de CSP.
La légère diminution de la proportion des greffes de sang placentaire dans l’activité globale se poursuit : 10,2% de greffes de sang placentaire en 2013, soit 191 en nombre absolu (contre 11,5% et 197 en 2012), après une période de forte croissance de 2003 à 2009, (ouverture de cette technique aux patients adultes).
La diminution porte sur l’activité de greffe non apparentée de sang placentaire : 222 en 2011 et 193 en 2012 contre 188 en 2013. Toutefois, la progression de cette activité en 10 ans est très forte : de 78 greffes en 2004 à 188 greffes en 2013, soit une progression de 141%. Le sang placentaire représente encore 17,2% des greffes non apparentées (Figure CSH G12).
Lorsqu’un patient avec une indication de greffe allogénique n’a pas de donneur familial ou non apparenté compatible (donneurs dits « standard »), alors les équipes de greffe font appel aux registres nationaux et internationaux de sang placentaire, ou bien commencent de façon encore préliminaire à développer une technique de greffe utilisant des donneurs partiellement compatibles ou « haplo-mismatch ». Les greffes avec ces « donneurs alternatifs » (donc sang placentaire ou adulte mismatch) font actuellement l’objet de nombreuses études au plan national et international, et leurs résultats aideront à toujours mieux préciser la place de chaque type de greffon et de technique de greffe pour les patients, notamment en fonction de leur pathologie et de leur état clinique.
L’activité d’allogreffe en 2013 se répartit dans 37 équipes dont certaines ont une activité adulte, d’autres une activité pédiatrique, et d’autres encore une activité mixte (adultes et enfants). L’activité la plus faible est de 7 greffes.
Le tableau CSH G9 rapporte l’activité d’allogreffe telle qu’elle a été déclarée par chaque centre. Dans la colonne centrale est notée l’activité extraite de la base de données ProMISe. En grisé sont indiqués les centres qui ont saisi dans ProMISe moins des trois quarts des greffes réalisées. Le tableau CSH G10 montre l’activité d’allogreffe de CSH par type de donneur, d’origine du greffon et par équipe en 2013. Le recours à un greffon prélevé chez un donneur non apparenté reste encore inégal entre les équipes (de 27% à 80%). Huit équipes réalisent 10 ou plus allogreffes non apparentées de sang placentaire, et 5 équipes se situent entre 6 et 9 greffes de sang placentaire par an.
Les indications d’allogreffe sont identiques, que le donneur soit apparenté ou non (Figure CSH G13, Figure CSH G14). Les hémopathies malignes représentent 88,1% des indications de greffe familiale et 93,1% des indications de greffe non apparentée. Les deux principales indications (Figure CSH G15-a) restent la leucémie aiguë myéloblastique et la leucémie aiguë lymphoblastique (respectivement 36,2% et 12,8% des allogreffes en 2013).
Les myélodysplasies représentent 9,8% des allogreffes en 2013, soit une progression de 36% par rapport à 2004 : ceci est à rapprocher de la moyenne d’âge plus élevée des patients atteints de myélodysplasie, qui ont accès à la greffe grâce aux nouvelles thérapeutiques utilisées avant la greffe comme les agents déméthylants et au développement des techniques de greffe avec conditionnement d’intensité réduite, notamment. Les indications d’allogreffe pour lymphomes non hodgkiniens et myélomes (Figure CSH G15-b), qui ont progressé de 1996 à 2000, sont stables depuis (respectivement 9,1% et 6,0% des allogreffes en 2013).
Le pourcentage de greffes réalisées après conditionnement d’intensité réduite (CIR) augmente (Figure CSH G16).
Dans ce cadre, la répartition des diagnostics (Figure CSH G17) est un peu différente de celle des greffes réalisées après conditionnement standard, avec notamment une part plus importante des hémopathies myéloïdes hors leucémie, comme les myélodysplasies (patients souvent âgés de plus de 55-60 ans), mais très peu de patients atteints de LAL (conditionnements standard utilisés le plus souvent en pédiatrie).
L’âge moyen des patients allogreffés avec un conditionnement réduit se stabilise (52 ans en 2013 contre 51 ans de 2010 à 2012, médiane : 57 ans en 2013 comme en 2012, contre 56 ans en 2011 et 55 ans en 2010). Celui des patients allogreffés avec un conditionnement standard est de 32 ans (médiane : 33 ans) en 2013, contre 30 ans de médiane et de moyenne en 2012.
Enfin, un total de 298 patients a reçu, après allogreffe, des injections de lymphocytes de leur donneur (Tableau CSH G12). La majorité de ces injections ont été réalisées dans le cadre de chimérisme mixte ou de rechute, et non pas de façon programmée.Tableau CSH G8. Activité d’allogreffe de CSH, par type de donneur et d’origine du greffon, en 2013*
|
Allogreffes apparentées |
Allogreffes non apparentées |
Total |
Moelle osseuse |
261 |
210 |
471 |
Sang périphérique |
518 |
692 |
1210 |
Sang placentaire |
3 |
188 |
191 |
Total |
782 |
1090 |
1872 |
Source : déclarations d’activité des centres de greffe
* voir paragraphe « matériel et méthodes – contrôle qualité »
Figure CSH G6. Evolution du nombre d’allogreffes de CSH selon le type de donneur*
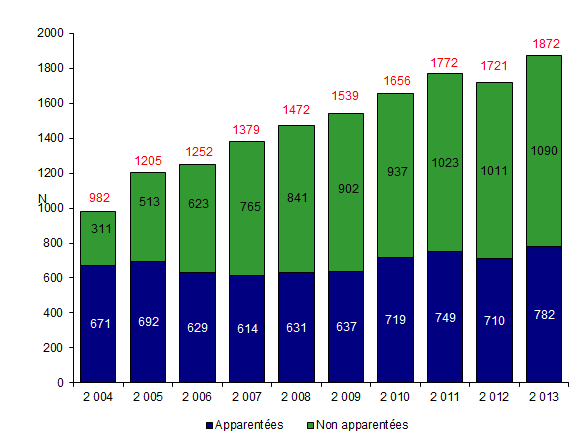
Source : déclarations d’activité des centres de greffe
* voir paragraphe « matériel et méthodes – contrôle qualité »
Figure CSH G7. Evolution du pourcentage d’allogreffes de CSH effectuées à partir d’un greffon d’un donneur non apparenté par rapport au nombre total d’allogreffes
Source : déclarations d’activité des centres de greffe
Figure CSH G8. Répartition des allogreffes de CSH selon le type du donneur
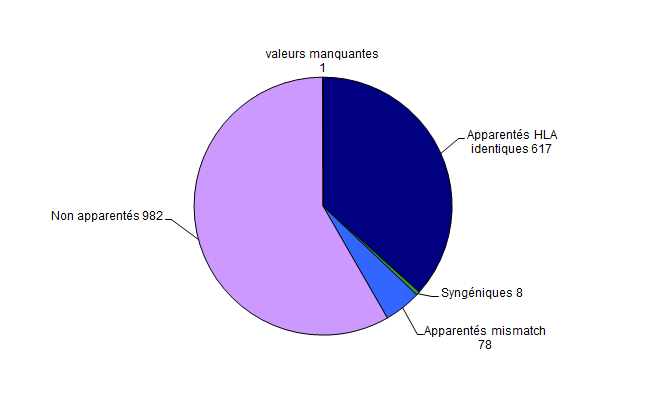
Source : Base ProMISe (extraction du 5 mai 2014)
Figure CSH G9. Evolution de l'âge moyen des patients ayant eu une allogreffe de CSH
Source : Base ProMISe (extraction du 5 mai 2014)
Figure CSH G10. Evolution de la répartition des sources de greffon des CSH allogéniques
Source : déclarations d’activité des centres de greffe
Figure CSH G11. Evolution de la répartition des sources de greffon des CSH allogéniques apparentées
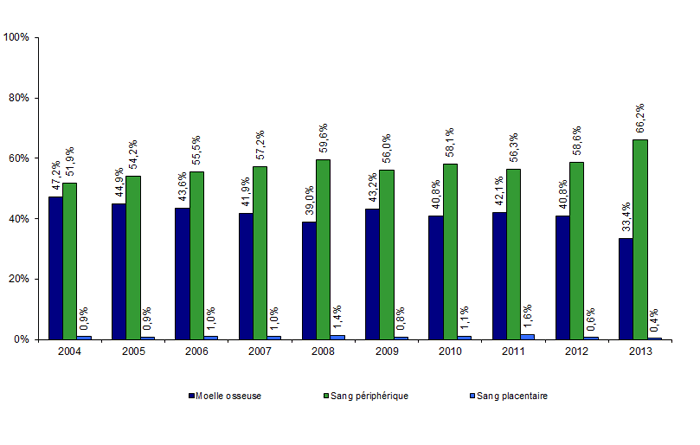
Source : déclarations d’activité des centres de greffe
Figure CSH G12. Evolution de la répartition des sources de greffon des CSH allogéniques non apparentées
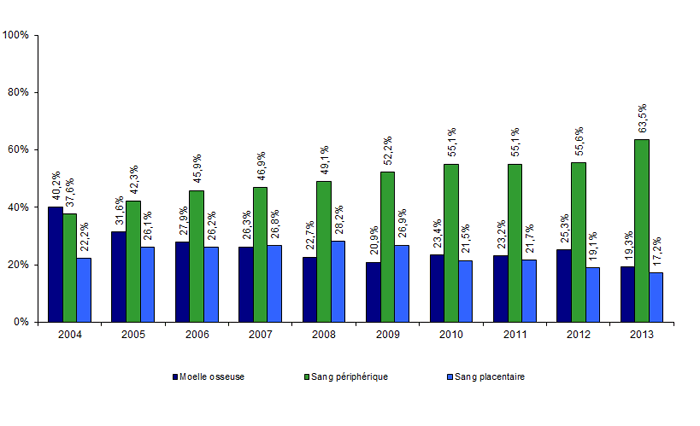
Source : déclarations d’activité des centres de greffe
Tableau CSH G9. Evolution de l'activité d'allogreffe de CSH par équipe
|
Nombre d'allogreffes |
ProMISe |
Nombre de patients |
||||||
|
2010 |
2011 |
2012 |
2013 |
2013 |
2010 |
2011 |
2012 |
2013 |
Amiens Hôpital Sud |
/ |
/ |
11 |
27 |
26 |
/ |
/ |
11 |
27 |
Angers CHU |
38 |
44 |
38 |
31 |
31 |
36 |
44 |
38 |
31 |
Besançon Hôpital Jean Minjoz |
60 |
53 |
52 |
44 |
44 |
60 |
53 |
49 |
42 |
Bordeaux Groupe Hospitalier Pellegrin |
15 |
24 |
19 |
22 |
22 |
14 |
24 |
18 |
21 |
Bordeaux Pessac Hôpital Haut Lévêque |
99 |
88 |
85 |
84 |
84 |
97 |
88 |
81 |
84 |
Brest Hôpital Augustin Morvan |
36 |
23 |
23 |
26 |
26 |
33 |
22 |
21 |
26 |
Caen CHU |
39 |
32 |
35 |
39 |
39 |
38 |
32 |
35 |
39 |
Clamart Hôpital d'Instruction des Armées |
15 |
28 |
19 |
29 |
4 |
15 |
28 |
19 |
29 |
Clermont-Ferrand |
40 |
48 |
44 |
53 |
12 |
40 |
47 |
44 |
51 |
Créteil Hôpital Henri Mondor |
39 |
40 |
36 |
33 |
33 |
39 |
38 |
35 |
33 |
Grenoble CHU |
37 |
55 |
46 |
49 |
49 |
37 |
51 |
45 |
48 |
Lille CHU Claude Huriez |
62 |
102 |
103 |
106 |
106 |
61 |
101 |
103 |
106 |
Lille Hôpital Jeanne de Flandre |
13 |
16 |
15 |
8 |
6 |
13 |
16 |
15 |
8 |
Limoges Centre Hospitalier Dupuytren |
23 |
21 |
27 |
24 |
20 |
22 |
21 |
27 |
23 |
Lyon Centre Hospitalier Lyon Sud |
71 |
88 |
74 |
73 |
73 |
70 |
87 |
71 |
72 |
Lyon Institut d'Hématologie et d'Oncologie Pédiatrique |
32 |
32 |
26 |
26 |
26 |
31 |
32 |
26 |
26 |
Marseille Hôpital de la Timone |
26 |
27 |
28 |
29 |
29 |
26 |
27 |
27 |
29 |
Marseille Institut Paoli Calmettes |
103 |
127 |
113 |
136 |
136 |
102 |
122 |
112 |
133 |
Montpellier Hôpital Saint-Eloi et Hôpital Arnaud de Villeneuve |
75 |
74 |
76 |
91 |
91 |
75 |
74 |
74 |
91 |
Nancy Hôpital d'Enfants |
41 |
53 |
50 |
40 |
40 |
41 |
52 |
50 |
40 |
Nantes Hôtel Dieu |
91 |
101 |
79 |
92 |
92 |
90 |
101 |
79 |
92 |
Nice Hôpital de l'Archet 1 |
32 |
33 |
46 |
45 |
28 |
31 |
32 |
46 |
45 |
Paris Hôpital Necker |
39 |
41 |
39 |
41 |
35 |
39 |
32 |
38 |
38 |
- service d'Hématologie Adultes |
34 |
28 |
36 |
43 |
40 |
34 |
27 |
36 |
41 |
Paris Hôpital Robert Debré |
60 |
60 |
62 |
64 |
63 |
58 |
59 |
60 |
58 |
Paris Hôpital Saint-Antoine |
14 |
41 |
37 |
73 |
31 |
13 |
39 |
37 |
71 |
Paris Hôpital Saint-Louis |
129 |
132 |
126 |
127 |
127 |
128 |
131 |
124 |
126 |
Paris Hôtel Dieu |
22 |
/ |
/ |
/ |
/ |
22 |
/ |
/ |
/ |
Paris La Pitié Salpetrière |
43 |
60 |
51 |
74 |
73 |
43 |
60 |
50 |
73 |
Poitiers Hôpital Jean Bernard |
38 |
26 |
23 |
32 |
31 |
35 |
26 |
22 |
32 |
Rennes CHU |
43 |
53 |
58 |
60 |
20 |
43 |
53 |
58 |
60 |
Rouen Centre Henri Becquerel |
31 |
28 |
26 |
27 |
27 |
31 |
28 |
25 |
27 |
Rouen Hôpital Charles Nicolle |
9 |
10 |
13 |
7 |
6 |
9 |
10 |
11 |
7 |
Saint-Étienne Institut de Cancérologie |
34 |
23 |
26 |
34 |
33 |
33 |
23 |
25 |
34 |
Strasbourg Hôpital de Hautepierre |
57 |
45 |
58 |
62 |
62 |
55 |
41 |
55 |
62 |
Toulouse Hôpital Purpan |
38 |
49 |
42 |
48 |
48 |
37 |
48 |
41 |
48 |
Tours Hôpital Bretonneau |
16 |
17 |
16 |
16 |
16 |
16 |
17 |
16 |
16 |
Villejuif Institut Gustave Roussy |
62 |
50 |
63 |
57 |
57 |
62 |
50 |
62 |
57 |
Total |
1656 |
1772 |
1721 |
1872 |
1686 |
1629 |
1736 |
1686 |
1846 |
Source : déclarations d’activité des centres de greffe
Tableau CSH G10. Activité d'allogreffe de CSH par type de donneur, d’origine du greffon et par équipe en 2013*
|
Moelle osseuse |
Sang périphérique |
Sang placentaire |
Total |
|||
|
apparentée |
non |
apparentée |
non |
apparentée |
non |
|
Amiens Hôpital Sud |
4 |
5 |
10 |
8 |
0 |
0 |
27 |
Angers CHU : |
3 |
2 |
10 |
15 |
0 |
1 |
31 |
Besançon Hôpital Jean Minjoz |
5 |
9 |
9 |
18 |
0 |
3 |
44 |
Bordeaux Groupe Hospitalier Pellegrin |
5 |
5 |
1 |
0 |
1 |
10 |
22 |
Bordeaux Pessac |
4 |
2 |
20 |
46 |
0 |
12 |
84 |
Brest Hôpital Augustin Morvan |
1 |
2 |
5 |
17 |
0 |
1 |
26 |
Caen CHU |
0 |
1 |
18 |
19 |
0 |
1 |
39 |
Clamart Hôpital d'Instruction des Armées |
2 |
6 |
7 |
7 |
0 |
7 |
29 |
Clermont-Ferrand |
4 |
4 |
18 |
24 |
0 |
3 |
53 |
Créteil Hôpital Henri Mondor |
1 |
4 |
9 |
15 |
0 |
4 |
33 |
Grenoble CHU: |
5 |
13 |
9 |
18 |
0 |
4 |
49 |
Lille CHU Claude Huriez |
25 |
30 |
9 |
36 |
0 |
6 |
106 |
Lille Hôpital Jeanne de Flandre |
4 |
2 |
0 |
1 |
0 |
1 |
8 |
Limoges Centre Hospitalier Dupuytren |
1 |
3 |
2 |
16 |
0 |
2 |
24 |
Lyon Centre Hospitalier Lyon Sud |
12 |
12 |
15 |
21 |
0 |
13 |
73 |
Lyon Institut d'Hématologie et d'Oncologie Pédiatrique |
9 |
11 |
0 |
2 |
0 |
4 |
26 |
Marseille Hôpital de la Timone : |
9 |
3 |
0 |
0 |
0 |
17 |
29 |
Marseille Institut Paoli Calmettes |
2 |
3 |
85 |
45 |
0 |
1 |
136 |
Montpellier Hôpital Saint-Eloi et Hôpital Arnaud de Villeneuve |
2 |
1 |
28 |
49 |
0 |
11 |
91 |
Nancy Hôpital d'Enfants |
7 |
5 |
7 |
20 |
0 |
1 |
40 |
Nantes Hôtel Dieu |
6 |
8 |
29 |
35 |
0 |
14 |
92 |
Nice Hôpital de l'Archet 1 |
7 |
10 |
3 |
18 |
0 |
7 |
45 |
Paris Hôpital Necker : |
22 |
12 |
2 |
4 |
0 |
1 |
41 |
- service d'Hématologie Adultes |
4 |
4 |
15 |
20 |
0 |
0 |
43 |
Paris Hôpital Robert Debré |
25 |
16 |
3 |
3 |
1 |
16 |
64 |
Paris Hôpital Saint-Antoine |
20 |
0 |
25 |
21 |
0 |
7 |
73 |
Paris Hôpital Saint-Louis : |
12 |
7 |
41 |
52 |
0 |
15 |
127 |
Paris La Pitié Salpetrière : |
15 |
6 |
29 |
24 |
0 |
0 |
74 |
Poitiers Hôpital Jean Bernard |
10 |
2 |
6 |
13 |
0 |
1 |
32 |
Rennes CHU |
12 |
10 |
18 |
14 |
0 |
6 |
60 |
Rouen Centre Henri Becquerel |
3 |
0 |
8 |
13 |
0 |
3 |
27 |
Rouen Hôpital Charles Nicolle |
2 |
2 |
0 |
1 |
0 |
2 |
7 |
Saint-Étienne Institut de Cancérologie |
2 |
1 |
11 |
16 |
0 |
4 |
34 |
Strasbourg Hôpital de Hautepierre |
6 |
4 |
21 |
26 |
1 |
4 |
62 |
Toulouse Hôpital Purpan : |
3 |
3 |
11 |
29 |
0 |
2 |
48 |
Tours Hôpital Bretonneau |
6 |
0 |
10 |
0 |
0 |
0 |
16 |
Villejuif Institut Gustave Roussy : |
1 |
2 |
24 |
26 |
0 |
4 |
57 |
Total |
261 |
210 |
518 |
692 |
3 |
188 |
1872 |
Source : déclarations d’activité des centres de greffe
* voir paragraphe « matériel et méthodes – contrôle qualité »
Tableau CSH G11. Evolution de l’activité d’allogreffe de CSH au niveau des schémas interrégionaux d’organisation sanitaire (SIOS)
|
Nombre d'allogreffes |
Nombre de patients |
||||||
|
2010 |
2011 |
2012 |
2013 |
2010 |
2011 |
2012 |
2013 |
SIOS Nord-Ouest |
153 |
188 |
203 |
214 |
152 |
187 |
200 |
214 |
SIOS Ouest |
262 |
264 |
237 |
257 |
253 |
263 |
234 |
257 |
SIOS Sud -Ouest |
175 |
182 |
173 |
178 |
170 |
181 |
167 |
176 |
SIOS Est |
158 |
151 |
160 |
146 |
156 |
146 |
154 |
144 |
SIOS Sud-Est |
214 |
246 |
216 |
235 |
211 |
240 |
211 |
231 |
SIOS Sud-Méditerranée |
236 |
261 |
263 |
301 |
234 |
255 |
259 |
298 |
SROS Ile de France |
458 |
480 |
469 |
541 |
453 |
464 |
461 |
526 |
France |
1656 |
1772 |
1721 |
1872 |
1629 |
1736 |
1686 |
1846 |
Source : déclarations d’activité des centres de greffe
Figure CSH G13. Répartition des indications en 2013 des allogreffes apparentées (n=691 patients)
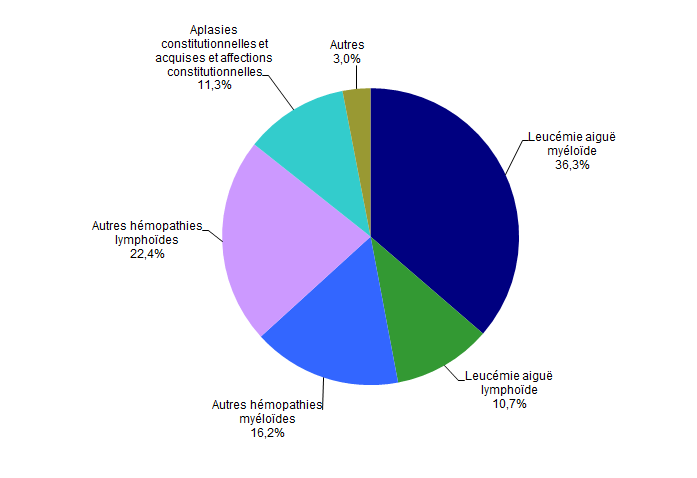
Source : Base ProMISe (extraction du 5 mai 2014)
Figure CSH G14. Répartition des indications en 2013 des allogreffes non apparentées (n=970 patients)
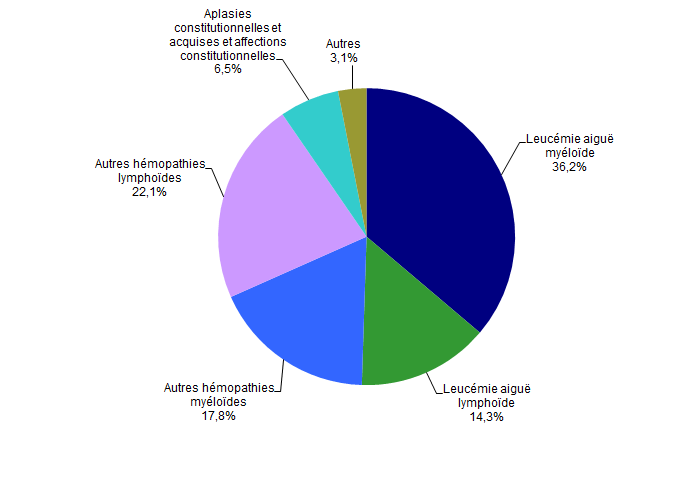
Source : Base ProMISe (extraction du 5 mai 2014)
Figure CSH G15a. Evolution de la répartition des indications d’allogreffe
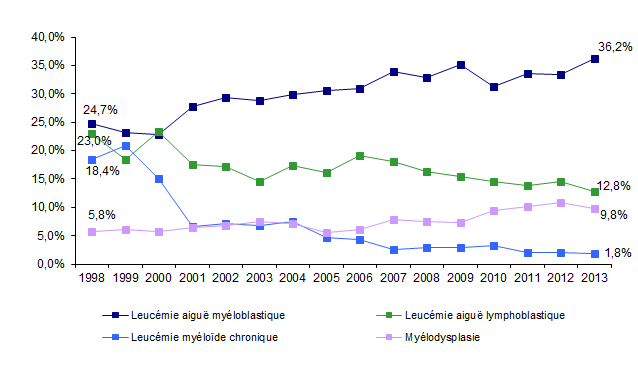
Source : Base ProMISe (extraction du 5 mai 2014)
Figure CSH G15b. Evolution de la répartition des indications d’allogreffe
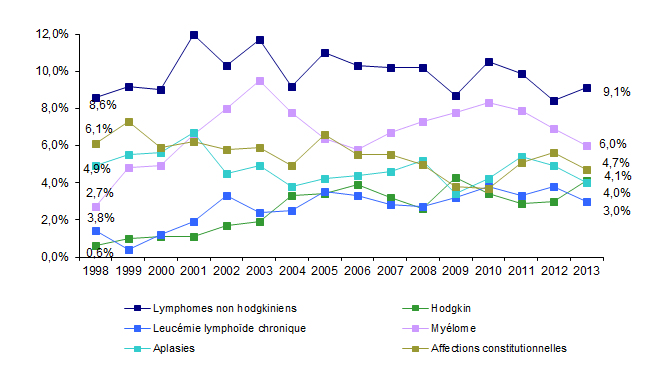
Source : Base ProMISe (extraction du 5 mai 2014)
Figure CSH G16. Evolution du pourcentage d’allogreffes de CSH réalisées après un conditionnement d’intensité réduite par rapport au nombre total d’allogreffes
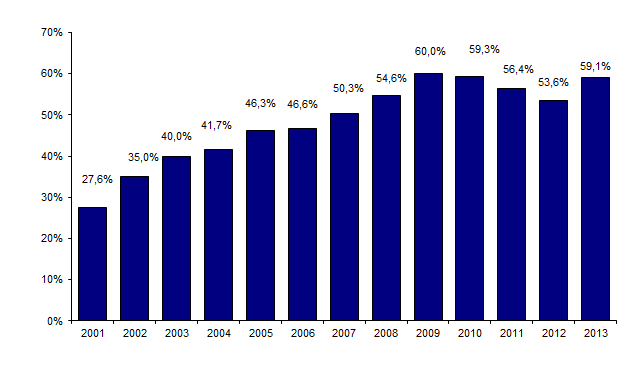
Source : déclarations d’activité des centres de greffe
Figure CSH G17. Répartition des indications en 2013 des allogreffes après conditionnement d’intensité réduite (n=932 patients)
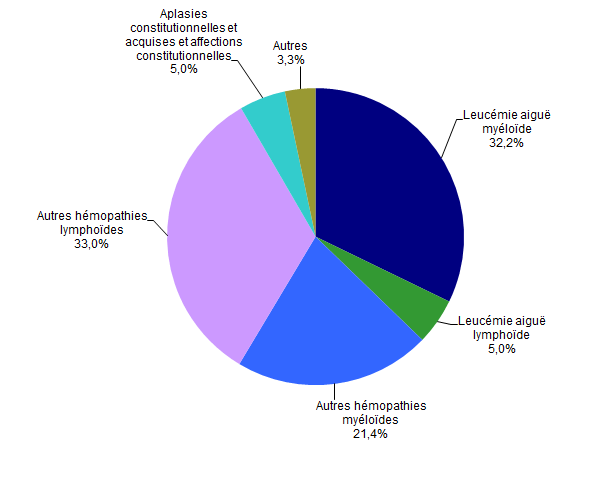
Source : Base ProMISe (extraction du 5 mai 2014)
Tableau CSH G12.Transfusions de lymphocytes du donneur (DLI) en 2013
Nombre de patients ayant eu |
Nombre de patients ayant eu |
Total |
||
De façon programmée |
De façon non programmée (rechute, chimérisme mixte) |
De façon programmée |
De façon non programmée (rechute, chimérisme mixte) |
|
23 |
162 |
22 |
91 |
298 |
Source : déclarations d’activité des centres de greffe
Activité de greffe allogénique pédiatrique
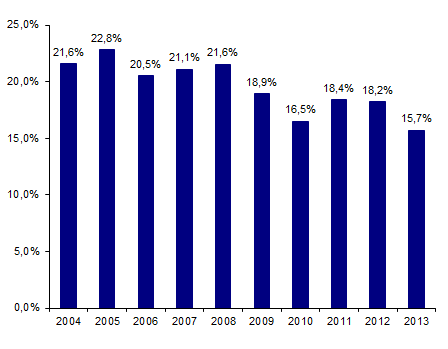
La part de l’activité d’allogreffe pédiatrique (âge inférieur à 18 ans) est stable depuis 4 ans et représente 15,7% des allogreffes en 2013. Cette activité a été évaluée sur les 1 686 allogreffes saisies dans ProMISe. Les données manquantes représentent les allogreffes non saisies dans ProMISe (n=186). Deux cent soixante-quatre (264) allogreffes de CSH ont été rapportées pour 254 patients de moins de 18 ans dans 20 centres.
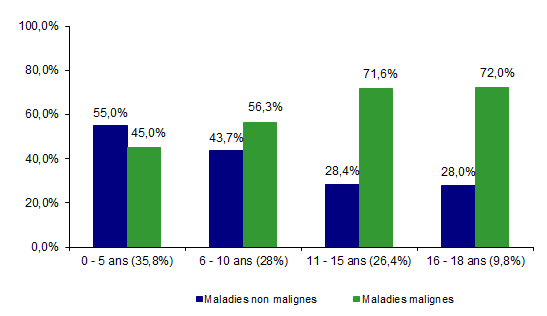
La part des maladies malignes dans les indications d’allogreffe chez les receveurs de moins de 18 ans (Figure CSH G19) représente 57,9% en 2013. Les maladies malignes augmentent en proportion avec l’augmentation de la classe d’âge (de 45% pour les moins de 5 ans à 72% pour les 16-18 ans).
La proportion de greffons issus de la moelle osseuse est, chez les receveurs mineurs, toujours majoritaire (62,5%) et plus élevée que dans la population générale (25,2%) en raison de l’interdiction de prélèvement des CSP mobilisées après G-CSF pour un donneur mineur (Tableau CSH G13). La part des greffes de sang placentaire (26,5 %) reste plus élevée que chez l’adulte (7,7%).
Figure CSH G18. Part de l’activité pédiatrique d’allogreffe de CSH depuis 2004
Source : Base ProMISe (extraction du 5 mai 2014)
Figure CSH G19. Proportion de maladies malignes en fonction de l’âge chez les 254 patients de moins de 18 ans ayant reçu une allogreffe en 2013
Source : Base ProMISe (extraction du 5 mai 2014)
Tableau CSH G13. Nombre d’allogreffes apparentées et non apparentées selon l’origine des cellules et le diagnostic chez les patients de moins de 18 ans, en 2013
|
Moelle osseuse |
Sang périphérique |
Sang placentaire |
Total |
|||
|
Apparenté |
Non apparenté |
Apparenté |
Non apparenté |
Apparenté |
Non apparenté |
|
Leucémie aigüe |
39 |
32 |
5 |
12 |
2 |
37 |
127 |
Maladies non malignes |
53 |
27 |
2 |
4 |
5 |
22 |
113 |
Autres |
7 |
7 |
3 |
3 |
0 |
4 |
24 |
Total |
99 |
66 |
10 |
19 |
7 |
63 |
264 |
Source : Base ProMISe (extraction du 5 mai 2014)
Etude de la survie des patients après allogreffe de cellules souches hématopoïétiques
Guide d’interprétation
La cohorte de base choisie pour cette étude est celle des treize dernières années : 2001-2013. Néanmoins, pour l’étude de certaines pathologies spécifiques (aplasies) ou de certaines sous-populations (allogreffes de sang placentaire), des cohortes plus larges ont été utilisées, incluant des années antérieures à 2001, pour avoir des effectifs suffisants.
Pour chaque courbe de survie, la largeur de la figure (échelle de l’axe des abscisses) représente le recul maximum théorique que l’on peut avoir pour un patient, compte tenu de la cohorte choisie. Par exemple pour la cohorte 2001-2013, l’axe des abscisses ira de 0 à 156 mois.
La courbe de survie s’arrête soit lorsqu’il n’y a plus assez de sujets encore à risque pour pouvoir calculer un taux de survie, soit au temps correspondant au dernier évènement (décès) de la cohorte. Par exemple, si le dernier évènement de la cohorte survient juste avant 5 ans, la courbe s’arrêtera avant 5 ans. Mais la survie à 5 ans peut quand même être calculée s’il y a encore à cette date assez de sujets à risque (elle figure dans le tableau sous la courbe de survie). En revanche, lorsque le taux de survie à 5 ans est « NO » dans le tableau en dessous de la courbe, cela signifie qu’il ne reste pas assez de sujets encore à risque à 5 ans pour calculer un taux de survie.
Par ailleurs, le nombre de sujets encore à risque nécessaire pour calculer un taux de survie a été calculé, selon les recommandations de Pocock (The Lancet, vol. 359, 2002), comme un pourcentage du nombre de sujets inclus dans la cohorte. Pour un même graphique, ce pourcentage est identique pour toutes les strates sur lesquelles on estime une courbe de survie. Il est de 15% pour tous les graphiques.
Etude globale selon la période de greffe
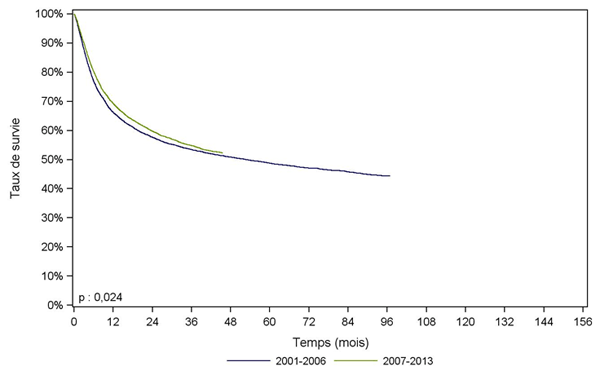
L’évolution des modalités de greffe a entrainé une amélioration de la survie, et toutes les cohortes ci-dessous montrent une survie supérieure à celle de 1995-2001 (non représentée). Un effet période est également observé à partir de 2001, que ce soit dans la population générale des malades allogreffés (Figure CSH G20), ou chez les patients greffés pour leucémie aiguë (Figure CSH G21) ou pour aplasie (Figure CSH G22). En effet, on constate une différence significative entre la survie des patients greffés de 2001 à 2006 et celle des patients greffés de 2007 à 2012.
Figure CSH G20. Survie des patients après allogreffe de CSH selon la période (cohorte 2001-2013)
période |
N |
Survie à 1 an |
Survie à 2 ans |
Survie à 5 ans |
Médiane de |
2001-2006 |
5745 |
66,3% |
57,7% |
48,7% |
52,7 |
nombre de sujets à risque* |
|
3676 |
3125 |
2161 |
|
2007-2013 |
10502 |
69,3% |
59,7% |
NO |
NO |
nombre de sujets à risque* |
|
5610 |
3666 |
636 |
|
[] : Intervalle de confiance
NO : non observable
* : Nombre de malades restant à observer pour chaque temps et pour lesquels aucun évènement n'est survenu
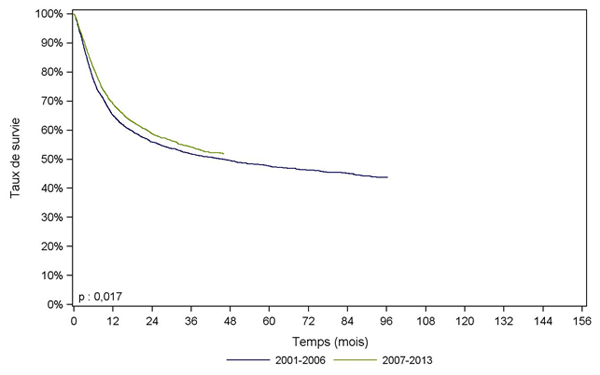
Figure CSH G21. Survie des patients après allogreffe pour leucémie aiguë myéloïde ou leucémie aiguë lymphoïde, selon la période (cohorte 2001-2013)
période |
N |
Survie à 1 an |
Survie à 2 ans |
Survie à 5 ans |
Médiane de |
2001-2006 |
2651 |
65,2% |
55,9% |
47,6% |
45,7 |
nombre de sujets à risque* |
|
1683 |
1415 |
1016 |
|
2007-2013 |
4874 |
69,2% |
58,8% |
NO |
NO |
nombre de sujets à risque* |
|
2612 |
1675 |
304 |
|
[] : Intervalle de confiance
NO : non observable
* : Nombre de malades restant à observer pour chaque temps et pour lesquels aucun évènement n'est survenu
Figure CSH G22. Survie des patients après allogreffe pour aplasie, selon la période (cohorte 2001-2013)
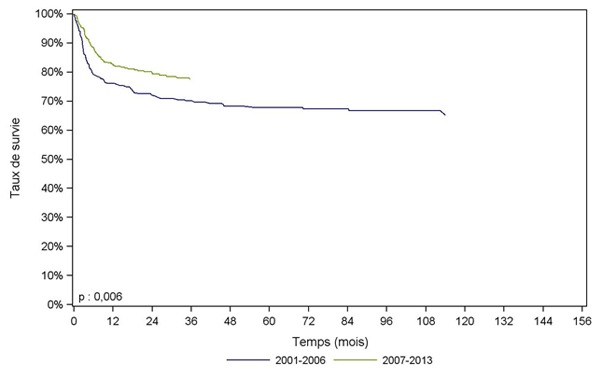
période |
N |
Survie à 1 an |
Survie à 2 ans |
Survie à 5 ans |
Médiane de |
2001-2006 |
264 |
76,1% |
72,1% |
67,9% |
NO |
nombre de sujets à risque* |
|
195 |
180 |
140 |
|
2007-2013 |
466 |
82,6% |
80,1% |
NO |
NO |
nombre de sujets à risque* |
|
296 |
213 |
50 |
|
[] : Intervalle de confiance
NO : non observable
* : Nombre de malades restant à observer pour chaque temps et pour lesquels aucun évènement n'est survenu
Etude de la survie des adultes greffés pour leucémies aiguës myéloïdes et lymphoïdes à partir de 2001, uniquement en première rémission complète
Dans les figures suivantes, le degré de disparité HLA des donneurs non apparentés n’a pas été pris en compte. De ce fait, les courbes de survie des adultes greffés avec un donneur non apparenté, et leurs différences avec celles des adultes ayant reçu des greffes apparentées sont à interpréter avec prudence, une partie des différences observées pouvant être expliquée par la disparité HLA (Figure CSH G23).
Figure CSH G23. Survie des adultes après allogreffe pour leucémie aiguë myéloïde en première rémission complète, selon le type de donneur (cohorte 2001-2013)
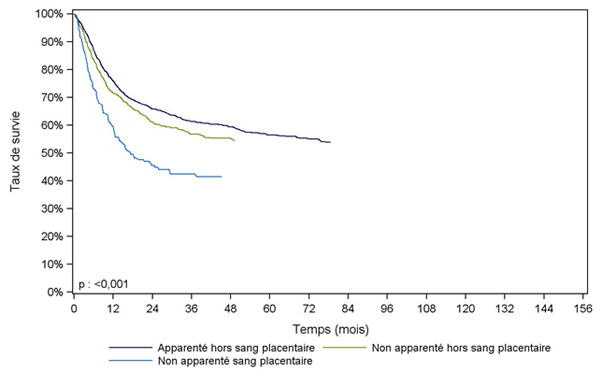
Type de donneur |
N |
Survie à 1 an |
Survie à 2 ans |
Survie à 5 ans |
Médiane de |
Apparenté hors sang placentaire |
1504 |
76,0% |
65,9% |
56,4% |
NO |
nombre de sujets à risque* |
|
967 |
724 |
368 |
|
Non apparenté hors sang placentaire |
996 |
71,8% |
61,2% |
NO |
NO |
nombre de sujets à risque* |
|
555 |
370 |
91 |
|
Non apparenté sang placentaire |
209 |
59,7% |
45,6% |
NO |
17,3 |
nombre de sujets à risque* |
|
101 |
66 |
22 |
|
[] : Intervalle de confiance
NO : non observable
* : Nombre de malades restant à observer pour chaque temps et pour lesquels aucun évènement n'est survenu
Figure CSH G24. Survie des adultes après allogreffe pour leucémie aiguë lymphoïde en première rémission complète, selon le type de donneur (cohorte 2001-2013)
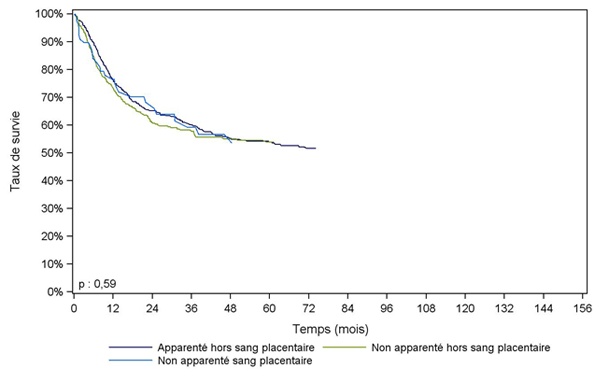
Type de donneur |
N |
Survie à 1 an |
Survie à 2 ans |
Survie à 5 ans |
Médiane de |
Apparenté hors sang placentaire |
583 |
76,3% |
65,2% |
53,9% |
NO |
nombre de sujets à risque* |
|
393 |
296 |
139 |
|
Non apparenté hors sang placentaire |
475 |
73,6% |
61,0% |
53,8% |
NO |
nombre de sujets à risque* |
|
288 |
193 |
77 |
|
Non apparenté sang placentaire |
77 |
76,4% |
68,1% |
53,6% |
NO |
nombre de sujets à risque* |
|
51 |
32 |
14 |
|
[] : Intervalle de confiance
NO : non observable
* : Nombre de malades restant à observer pour chaque temps et pour lesquels aucun évènement n'est survenu
Etude de la survie des enfants après allogreffe de CSH
Les différences de survie importantes concernant la cohorte des enfants greffés avec des sangs placentaires non apparentés par rapport à ceux greffés avec des donneurs, apparentés ou non, sont à interpréter avec prudence ; en effet, les groupes d’enfants greffés avec sang placentaire sont de faible effectif et peuvent être différents en ce qui concerne certains facteurs pronostiques, comme le statut de la maladie à la greffe (souvent plus avancé pour les enfants greffés avec des sangs placentaires) et ceci peut influer sur la survie globale.
Dans les figures CSH G25, CSH G26, les effectifs sont trop faibles pour distinguer les différents types de rémission complète. Il faut noter que parmi les 130 patients ayant reçu du sang placentaire non apparenté pour leucémie aiguë myéloïde, seuls 65 patients étaient en première rémission complète.
Figure CSH G25. Survie des enfants après allogreffe pour leucémie aiguë myéloïde en rémission complète, selon le type de donneur (cohorte 2001-2013)
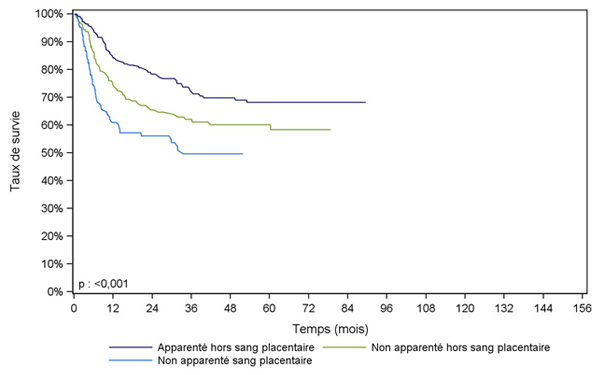
Type de donneur |
N |
Survie à 1 an |
Survie à 2 ans |
Survie à 5 ans |
Médiane de |
Apparenté hors sang placentaire |
230 |
84,7% |
78,5% |
68,2% |
NO |
nombre de sujets à risque* |
|
169 |
144 |
72 |
|
Non apparenté hors sang placentaire |
159 |
74,5% |
65,5% |
60,2% |
NO |
nombre de sujets à risque* |
|
104 |
81 |
38 |
|
Non apparenté sang placentaire |
130 |
61,0% |
56,2% |
NO |
33,5 |
nombre de sujets à risque* |
|
67 |
52 |
18 |
|
[] : Intervalle de confiance
NO : non observable
* : Nombre de malades restant à observer pour chaque temps et pour lesquels aucun évènement n'est survenu
Figure CSH G26. Survie des enfants après allogreffe pour leucémie aiguë lymphoïde en rémission complète, selon le type de donneur (cohorte 2001-2013)
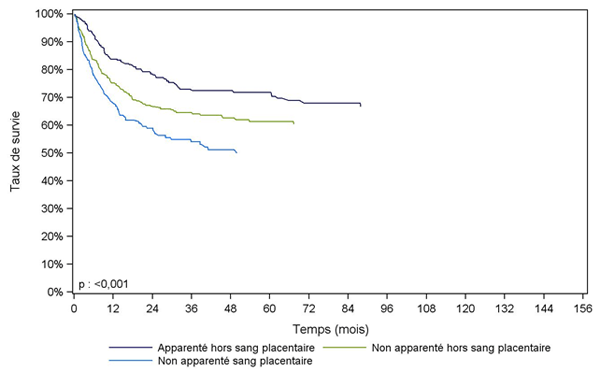
Type de donneur |
N |
Survie à 1 an |
Survie à 2 ans |
Survie à 5 ans |
Médiane de |
Apparenté hors sang placentaire |
293 |
83,7% |
78,4% |
71,8% |
NO |
nombre de sujets à risque* |
|
215 |
184 |
103 |
|
Non apparenté hors sang placentaire |
334 |
75,1% |
66,7% |
61,3% |
NO |
nombre de sujets à risque* |
|
220 |
160 |
77 |
|
Non apparenté sang placentaire |
220 |
68,3% |
58,9% |
NO |
49,9 |
nombre de sujets à risque* |
|
133 |
91 |
32 |
|
[] : Intervalle de confiance
NO : non observable
* : Nombre de malades restant à observer pour chaque temps et pour lesquels aucun évènement n'est survenu
Etude sur les aplasies selon l’origine (acquise ou constitutionnelle)
Les figures suivantes (Figures CSH G27, CSH G28) ont été réalisées à partir d’une cohorte large (1995-2013) en raison du faible effectif de patients allogreffés pour aplasie. L’absence de prise en compte des disparités HLA des donneurs non apparentés rend l’interprétation de ces courbes délicate.Figure CSH G27. Survie des patients après allogreffe pour aplasie acquise, selon le type de donneur (cohorte 1995-2013)
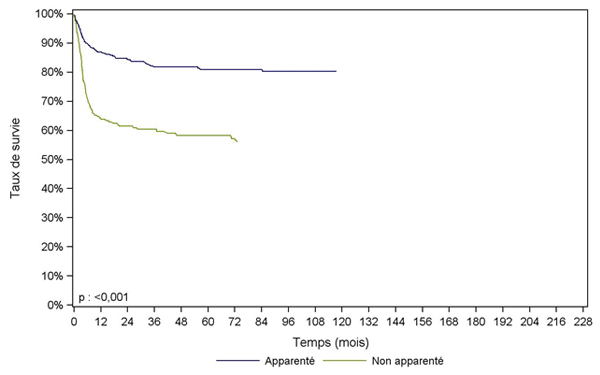
Type de donneur |
N |
Survie à 1 an |
Survie à 2 ans |
Survie à 5 ans |
Médiane de |
Apparenté |
464 |
86,9% |
84,5% |
80,9% |
NO |
nombre de sujets à risque* |
|
348 |
299 |
175 |
|
Non apparenté |
256 |
64,3% |
61,4% |
58,3% |
NO |
nombre de sujets à risque* |
|
144 |
121 |
66 |
|
[] : Intervalle de confiance
NO : non observable
* : Nombre de malades restant à observer pour chaque temps et pour lesquels aucun évènement n'est survenu
Figure CSH G28. Survie des patients après allogreffe pour aplasie constitutionnelle, selon le type de donneur (cohorte 1995-2013)
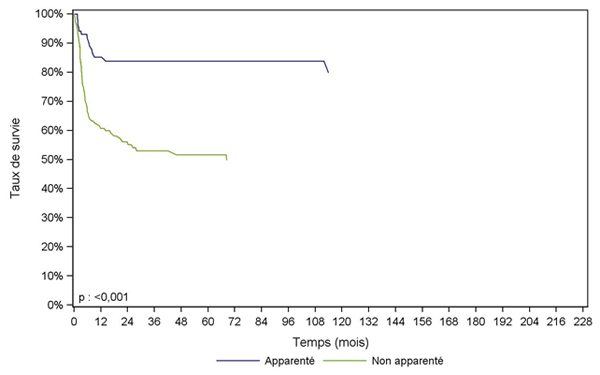
Type de donneur |
N |
Survie à 1 an |
Survie à 2 ans |
Survie à 5 ans |
Médiane de |
Apparenté |
87 |
85,1% |
83,8% |
83,8% |
NO |
nombre de sujets à risque* |
|
63 |
50 |
34 |
|
Non apparenté |
134 |
60,8% |
56,2% |
51,6% |
68,4 |
nombre de sujets à risque* |
|
72 |
55 |
31 |
|
[] : Intervalle de confiance
NO : non observable
* : Nombre de malades restant à observer pour chaque temps et pour lesquels aucun évènement n'est survenu
Etude de la survie des patients ayant reçu une greffe après un conditionnement d’intensité réduite
L’âge moyen des patients allogreffés avec un conditionnement réduit est de 52 ans (médiane : 57 ans), tandis que celui des patients allogreffés avec un conditionnement standard est de 32 ans (médiane : 33 ans).
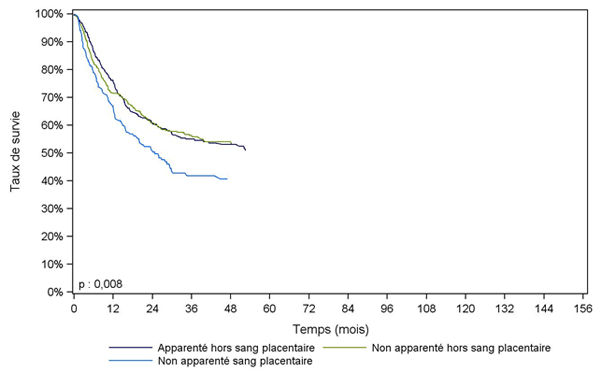
Parmi les figures suivantes seule celle sur les patients greffés pour leucémie aiguë myéloïde (cohorte 2007-2013) distingue la catégorie des allogreffes de sang placentaire non apparentées (pour les autres courbes, l’effectif de cette catégorie est trop faible pour l’individualiser, elle est donc incluse dans la catégorie « non apparentées »).
Concernant les patients greffés entre 2007 et 2013 pour leucémie aiguë myéloïde en rémission complète, avec un conditionnement atténué (Figure CSH G30), l’interprétation de la survie inférieure observée avec les greffes non apparentées de sang placentaire doit être nuancée par la situation des patients présentant une indication pour ce type de greffe : la plupart des patients présentent des facteurs de mauvais pronostic dits « haut risque » au niveau des caractéristiques de la maladie au diagnostic (faible chimiosensibilité initiale, caryotype défavorable, anomalies détectées au niveau moléculaire), ce qui implique un risque de rechute plus élevé après la greffe.
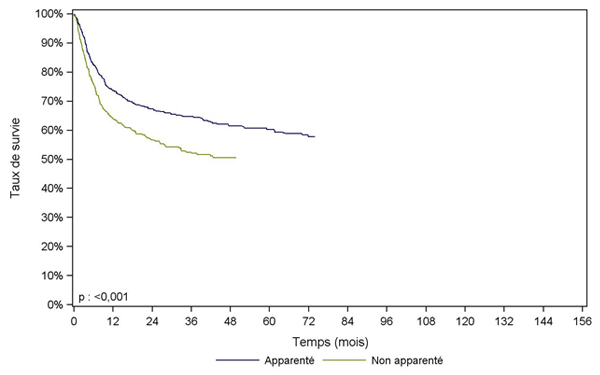
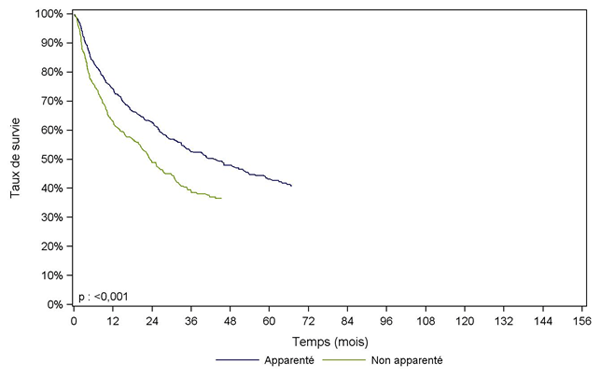
Pour les lymphomes et myélomes (Figure CSH G31, G32), les patients ayant reçu une greffe avec un donneur apparenté ont une meilleure survie que les autres patients. Un effet période a été étudié, mais comme la même différence entre donneurs apparentés et non apparentés est observée avant ou après 2007, nous avons préféré, pour la lisibilité des courbes, les présenter sur l’ensemble de la cohorte 2001-2013.Figure CSH G29. Survie des patients après allogreffe avec conditionnement atténué pour leucémie aiguë myéloïde en rémission complète (cohorte 2001-2006)
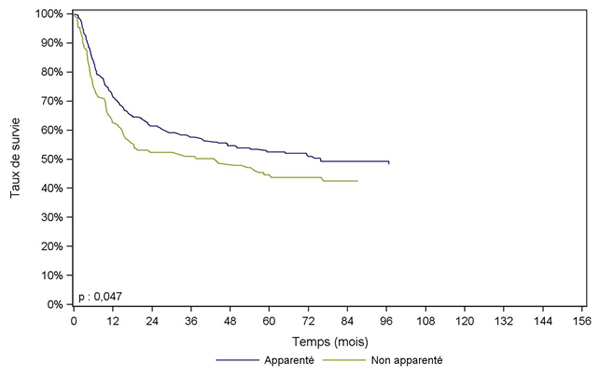
Type de donneur |
N |
Survie à 1 an |
Survie à 2 ans |
Survie à 5 ans |
Médiane de |
Apparenté |
274 |
71,8% |
61,6% |
52,6% |
75,7 |
nombre de sujets à risque* |
|
191 |
159 |
116 |
|
Non apparenté |
149 |
62,7% |
52,4% |
44,6% |
43,8 |
nombre de sujets à risque* |
|
92 |
75 |
49 |
|
[] : Intervalle de confiance
NO : non observable
* : Nombre de malades restant à observer pour chaque temps et pour lesquels aucun évènement n'est survenu
Figure CSH G30. Survie des patients après allogreffe avec conditionnement atténué pour leucémie aiguë myéloïde en rémission complète (cohorte 2007-2013)
Type de donneur |
N |
Survie à 1 an |
Survie à 2 ans |
Survie à 5 ans |
Médiane de |
Apparenté hors sang placentaire |
450 |
76,1% |
60,7% |
NO |
NO |
nombre de sujets à risque* |
|
309 |
192 |
46 |
|
Non apparenté hors sang placentaire |
572 |
71,5% |
60,8% |
NO |
NO |
nombre de sujets à risque* |
|
373 |
234 |
28 |
|
Non apparenté sang placentaire |
186 |
66,3% |
51,0% |
NO |
24,7 |
nombre de sujets à risque* |
|
115 |
76 |
11 |
|
[] : Intervalle de confiance
NO : non observable
* : Nombre de malades restant à observer pour chaque temps et pour lesquels aucun évènement n'est survenu
Figure CSH G31. Survie des patients après allogreffe avec conditionnement atténué pour lymphome (cohorte 2001-2013)
Type de donneur |
N |
Survie à 1 an |
Survie à 2 ans |
Survie à 5 ans |
Médiane de |
Apparenté |
615 |
73,7% |
67,3% |
60,3% |
NO |
nombre de sujets à risque* |
|
387 |
312 |
136 |
|
Non apparenté |
514 |
64,1% |
56,8% |
NO |
NO |
nombre de sujets à risque* |
|
264 |
198 |
47 |
|
[] : Intervalle de confiance
NO : non observable
* : Nombre de malades restant à observer pour chaque temps et pour lesquels aucun évènement n'est survenu
Figure CSH G32. Survie des patients après allogreffe avec conditionnement atténué pour myélome (cohorte 2001-2013)
Type de donneur |
N |
Survie à 1 an |
Survie à 2 ans |
Survie à 5 ans |
Médiane de |
Apparenté |
551 |
74,3% |
62,9% |
43,1% |
43,1 |
nombre de sujets à risque* |
|
354 |
267 |
101 |
|
Non apparenté |
397 |
63,0% |
48,9% |
NO |
23,4 |
nombre de sujets à risque* |
|
220 |
145 |
32 |
|
[] : Intervalle de confiance
NO : non observable
* : Nombre de malades restant à observer pour chaque temps et pour lesquels aucun évènement n'est survenu